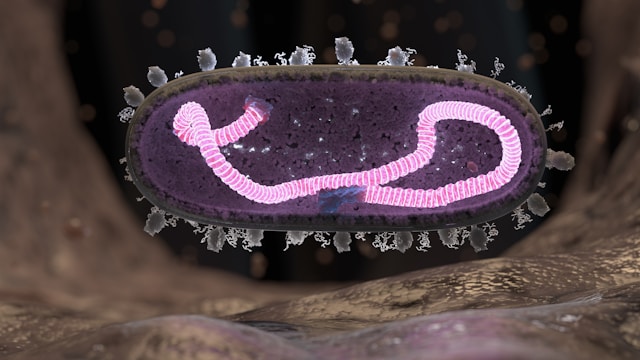
Le microbiote intestinal est souvent perçu comme un simple ensemble de bactéries résidant dans notre tube digestif, mais il constitue en réalité un écosystème complexe et dynamique, essentiel à notre santé globale. En 2026, la recherche continue de révéler comment l’alimentation influence directement la composition, la diversité et l’activité métabolique de ces micro-organismes, en mettant en lumière l’importance cruciale des fibres, des protéines, mais aussi des interactions entre différents types de bactéries. Ce que nous choisissons de manger façonne l’équilibre bactérien de notre intestin, modulant ainsi des fonctions vitales telles que la digestion, l’immunité, voire même notre humeur et notre poids.
Le rôle primordial des fibres alimentaires pour un microbiote intestinal équilibré
Les fibres alimentaires jouent un rôle central dans l’alimentation du microbiote intestinal, agissant comme un carburant indispensable pour la survie et la diversité des bactéries qui peuplent notre intestin. Ces longues chaînes polysaccharidiques, présentes en abondance dans des aliments tels que les légumes frais ou secs, les fruits et les céréales complètes, ne sont pas directement digérées par notre organisme. À la place, elles sont fermentées par une multitude d’espèces bactériennes, chacune disposant d’enzymes spécifiques à différentes étapes du processus de dégradation.
Ce mécanisme en chaîne montre que la diversité bactérienne est essentielle : chaque groupe bactérien scinde les fibres en fragments de plus en plus petits, jusqu’à ce que des acides gras à courte chaîne (AGCC), tels que le butyrate, le propionate et l’acétate, soient produits. Ces AGCC jouent un rôle majeur dans la santé intestinale en régulant les inflammations et en servant de source d’énergie aux cellules épithéliales du côlon. Par exemple, le butyrate favorise la régénération de la muqueuse intestinale, ce qui fortifie la barrière contre les agents pathogènes. Par ailleurs, ces acides gras contribuent à la satiété en stimulant la production de glucose dans l’intestin, jouant ainsi un rôle dans la régulation du poids corporel en limitant la surconsommation alimentaire.
Il est important de souligner que la diminution de l’apport en fibres, fréquente dans les régimes occidentaux modernes, compromet non seulement l’équilibre bactérien mais aussi leur nombre. Cette perte de diversité favorise une instabilité du microbiote, parfois appelée dysbiose, susceptible d’aggraver les troubles digestifs et inflammatoires. Des chercheurs de l’Inra ont démontré que les individus ayant une alimentation riche en fibres présentent une meilleure stabilité de leur microbiote, avec un nombre plus élevé et plus varié d’espèces bactériennes, contribuant à une santé intestinale optimisée.
De façon innovante, de nouvelles études ont révélé que cette fermentation ne se limite pas au côlon, comme on le pensait auparavant. Grâce à la métagénomique, on sait désormais qu’une partie de cette dégradation commence dès l’iléon, une région de l’intestin grêle. Cette découverte a des implications majeures, remettant en question les approches traditionnelles de la nutrition et invitant à reconsidérer le rôle direct des fibres dans différentes zones du tube digestif.
Pour illustrer ce processus, le projet Modaltub, piloté par l’Inra, a mis au point des modèles mathématiques et des digesteurs artificiels qui simulent la déconstruction alimentaire depuis la bouche jusqu’au côlon. En croquant dans une pomme, par exemple, les fibres, les protéines et les parois cellulaires subissent une dégradation progressive orchestrée par ces bactéries et enzymes, permettant l’assimilation des nutriments essentiels tout en évacuant les résidus inutiles. Ces outils innovants permettent aussi de tester les effets de divers aliments et de paramètres physiologiques, ouvrant la voie à une nutrition personnalisée, centrée sur le microbiote intestinal.
Impact de l’alimentation protéique et son métabolisme sur la santé de votre microbiote intestinal
La consommation excessive de protéines, une tendance marquée dans les sociétés contemporaines, soulève des questions importantes sur ses répercussions sur le microbiote intestinal. Alors que les besoins en protéines peuvent être augmentés pour certains groupes, tels que les sportifs ou les personnes âgées, la moyenne française consomme en général environ 1,7 fois la quantité recommandée, et cela influence directement la santé digestive.
Une partie des protéines ingérées en excès n’est ni digérée ni absorbée dans l’intestin grêle, ce qui entraîne leur passage dans le côlon où elles subissent une fermentation bactérienne. Ce métabolisme produit des molécules comme le sulfure d’hydrogène ou le p-cresol, reconnues pour leur toxicité potentielle sur les cellules intestinales. Ces composés peuvent perturber la muqueuse intestinale, altérer l’intégrité de la barrière épithéliale et même modifier l’ADN des cellules protectrices de l’intestin. Cette altération peut contribuer à une inflammation locale chronique qui, en s’étendant dans la circulation sanguine, impacte d’autres organes comme les reins.
Ce phénomène explique en partie pourquoi les régimes hyperprotéinés amincissants, bien qu’efficaces à court terme, peuvent poser des risques pour la santé à long terme si leur composition et leur équilibre ne sont pas bien maîtrisés. Par exemple, des personnes suivant ces régimes observent parfois des troubles digestifs, une inflammation accrue, voire une altération du microbiote, qui perd en diversité et en fonctions équilibrantes.
Les recherches actuelles tendent donc à affiner les recommandations alimentaires, notamment pour les populations sensibles, afin d’équilibrer les apports protéiques de manière à maximiser les bénéfices – maintien musculaire, performances sportives – tout en limitant les effets néfastes sur la flore intestinale. C’est un véritable défi, car chaque individu présente un microbiote unique et réagit différemment aux mêmes apports nutritionnels.
Pour approfondir cette problématique, des études ont recours à des analyses métabolomiques qui identifient précisément les molécules libérées par les bactéries lors de la fermentation protéique. Ces investigations permettent de mieux comprendre les interactions entre certaines bactéries productrices de composés toxiques et d’autres espèces bénéfiques, donnant ainsi des pistes pour développer des probiotiques ciblés capables de contrecarrer ces effets nocifs.
Déséquilibres du microbiote intestinal : lien avec l’obésité, l’inflammation et les pathologies digestives
L’équilibre du microbiote intestinal joue un rôle fondamental dans la gestion de l’énergie et la prévention de certaines maladies métaboliques. Lorsqu’il fonctionne bien, il améliore la digestion et l’assimilation des nutriments, mais un déséquilibre néfaste, ou dysbiose, peut altérer ces fonctions et contribuer au développement de l’obésité.
Des recherches comparatives entre individus obèses et non obèses ont mis en lumière des différences importantes dans la richesse et la diversité bactérienne. Les personnes souffrant d’obésité sévère présentent souvent une diminution de la diversité bactérienne, accompagnée d’une prolifération d’espèces bactériennes moins protectrices. Ce microbiote altéré perd ses capacités à réguler la quantité d’énergie absorbée, ce qui favorise un excès d’apport qui se traduit par un stockage accru de graisses au niveau des cellules adipeuses.
Par ailleurs, cette modification du microbiote engendre une inflammation chronique de bas grade dans l’intestin et les tissus périphériques, renforcée par la perméabilité intestinale accrue. Ce phénomène facilite le passage de lipopolysaccharides (LPS), composants bactériens inflammatoires, dans le sang, aggravant ainsi l’état métabolique et contribuant à des pathologies comme le diabète de type 2 et les maladies cardiovasculaires.
Impossible d’ignorer aussi l’impact du microbiote sur les troubles fonctionnels digestifs tels que le syndrome de l’intestin irritable (SII). Cette affection, touchant 10 à 20 % de la population française, est caractérisée par un déséquilibre bactérien qui modifie la production métabolique des bactéries : par exemple, une baisse de la production de butyrate et une augmentation des composés gazeux inflammatoires engendrent douleurs abdominales et troubles du transit.
On est désormais capable de cibler certains micro-organismes intervenant dans ces mécanismes et d’envisager des traitements innovants basés sur des probiotiques spécifiques capables de restaurer un équilibre favorable. Par exemple, une bactérie isolée a montré des capacités à réduire les produits gazeux nuisibles et à améliorer significativement les symptômes chez les patients touchés.